Ngày 8 tháng 12 , 2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã phê duyệt Casgevy và Lyfgenia, hai liệu pháp chỉnh sửa gen tế bào được sử dụng lần đầu tiên để điều trị bệnh hồng cầu hình liềm (SCD) đối với bệnh nhân từ 12 tuổi trở lên. Một trong hai liệu pháp này, Casgevy là liệu pháp sử dụng công nghệ chỉnh sửa gen mới lần đầu tiên được FDA phê chuẩn, đánh dấu một bước tiến đột phá trong lĩnh vực điều trị bằng liệu pháp gen.
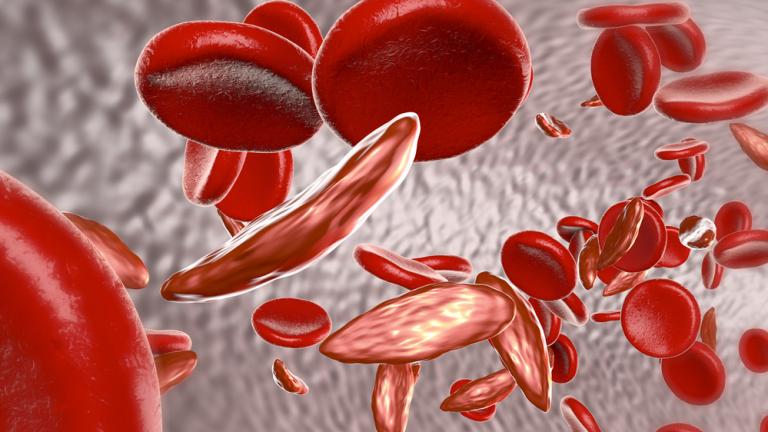
Bệnh hồng cầu hình liềm là một nhóm bệnh rối loạn máu di truyền ảnh hưởng đến khoảng 100.000 người ở Hoa Kỳ. Bệnh này phổ biến nhất ở người Mỹ gốc Phi và ít phổ biến hơn ở người Mỹ gốc Tây Ban Nha. Vấn đề chính của bệnh hồng cầu hình liềm là sự đột biến của huyết sắc tố (hemoglobin)- một loại protein trong tế bào hồng cầu có vai trò cung cấp oxy cho các mô của cơ thể. Đột biến này làm cho tế bào hồng cầu phát triển thành dạng hình lưỡi liềm hoặc hình liềm, là các tế bào có ảnh hưởng hạn chế quá trình lưu thông mạch máu, giảm khả năng cung cấp oxy tới các tổ chức mô của cơ thể, dẫn đến các cơn đau và tổn thương cơ quan (biến cố tắc mạch -VOE) hoặc cơn tắc mạch (VOC). Sự tái diễn các triệu chứng này có thể gây các rối loạn có nguy cơ đe dọa tính mạng và tử vong sớm.
“Bệnh hồng cầu hình liềm là một chứng rối loạn máu hiếm gặp, gây suy nhược và đe dọa tính mạng nhưng chưa có được các trị liệu đáp ứng thỏa đáng. Chúng tôi rất vui mừng được thúc đẩy liệu pháp này, đặc biệt đối với những bệnh nhân đang bị ảnh hưởng nghiêm trọng, bằng cách phê duyệt hai liệu pháp điều trị trên cơ sở chỉnh sửa gen tế bào hiện nay, ” Nicole Verdun, MD, giám đốc Văn phòng Sản phẩm Trị liệu thuộc Trung tâm Nghiên cứu và Đánh giá Sinh học của FDA cho biết. “Liệu pháp gen hứa hẹn mang lại những phương pháp điều trị đúng mục tiêu và hiệu quả hơn, đặc biệt đối với trường hợp các bệnh hiếm gặp mà các phương pháp điều trị hiện tại còn có hiệu quả hạn chế.”
Casgevy – liệu pháp trên cơ sở chỉnh sử gen tế bào, được phê duyệt để điều trị bệnh hồng cầu hình liềm ở bệnh nhân từ 12 tuổi trở lên bị các cơn tắc mạch tái phát. Casgevy là liệu pháp chỉnh sửa gen tế bào gốc tạo máu (máu) của bệnh nhân bằng công nghệ CRISPR/Cas9 được FDA phê chuẩn lần đầu tiên.
CRISPR/Cas9 có thể được sử dụng để cắt DNA theo yêu cầu cụ thể, cho phép chỉnh sửa DNA (loại bỏ, thêm hoặc thay thế) chính xác ở khu vực bị cắt. Sau khi được cấy truyền trở lại bệnh nhân các tế bào gốc máu đã được chỉnh sửa gen sẽ được tiếp nhận, nhân lên trong tủy xương, sẽ thúc đẩy quá trình sản xuất huyết sắc tố bào thai (HbF), một loại huyết sắc tố có tác dụng giúp cho việc vận chuyển oxy được dễ dàng. Ở những bệnh nhân mắc bệnh hồng cầu hình liềm, sự gia tăng nồng độ HbF sẽ ngăn ngừa sự hình thành tế bào hồng cầu hình liềm.
Lyfgenia là một liệu pháp trên cơ sở chỉnh sửa gen tế bào. Lyfgenia sử dụng vectơ lentivirus (phương tiện chuyển gen) để chỉnh sửa gen và được chấp thuận để điều trị bệnh hồng cầu hình liềm đối với bệnh nhân từ 12 tuổi trở lên và có tiền sử tắc mạch. Với Lyfgenia, tế bào gốc máu của bệnh nhân được chỉnh sửa gen để tạo ra HbA T87Q , một loại huyết sắc tố có chức năng tương tự như huyết sắc tố A của người bình thường không mắc bệnh hồng cầu hình liềm. Các tế bào hồng cầu chứa HbA T87Q có tác dụng giảm nguy cơ bị hình liềm và tắc nghẽn mạch máu sẽ được truyền lại vào cơ thể bệnh nhân.
Cả hai sản phẩm trên đều được làm từ tế bào gốc máu của chính bệnh nhân (tế bào gốc tự thân), đã được sửa đổi và được truyền lại dưới dạng tiêm truyền một lần, như một phần của quá trình cấy ghép tế bào gốc tạo máu (máu). Trước khi điều trị, tế bào tự thân sẽ được lấy ra khỏi cơ thể và sau đó bệnh nhân phải trải qua quá trình điều trị suy tủy (hóa trị liệu liều cao). Đây là quá trình loại bỏ các tế bào khỏi tủy xương để chúng có thể được thay thế bằng các tế bào gốc tự thân đã chỉnh sửa bằng phương pháp Casgevy và Lyfgenia . Bệnh nhân được điều trị bằng Casgevy hoặc Lyfgenia sẽ được theo dõi dài hạn để đánh giá tính an toàn và hiệu quả của từng sản phẩm.
Peter Marks, MD, Ph.D., Giám đốc Trung tâm Nghiên cứu và Đánh giá Sinh học của FDA cho biết: “Những phê duyệt này thể hiện một tiến bộ y tế quan trọng trong việc sử dụng các liệu pháp tiên tiến chỉnh sửa gen tế bào để chế ngự có hiệu quả các loại bệnh nghiêm trọng và để cải thiện sức khỏe cộng đồng”. “Các quyết định “Hiện hành” này tuân thủ các đánh giá nghiêm ngặt về dữ liệu khoa học và lâm sàng cần thiết để hỗ trợ việc phê duyệt, phản ánh cam kết của FDA trong việc tạo điều kiện phát triển các phương pháp điều trị an toàn và hiệu quả với điều kiện có tác động nghiêm trọng đến sức khỏe con người.”
Casgevy hỗ trợ dữ liệu
Tính an toàn và hiệu quả của Casgevy đã được đánh giá trong các thử nghiệm lâm sàng đơn nhánh và đa trung tâm ở bệnh nhân trưởng thành và thanh thiếu niên mắc SCD. Bệnh nhân có tiền sử mắc ít nhất hai VOC nghiêm trọng dựa theo quy trình xác định trong mỗi hai năm trước khi sàng lọc. Kết quả chính về hiệu quả là không còn các đợt VOC nghiêm trọng trong ít nhất 12 tháng liên tục trong thời gian theo dõi 24 tháng. Tổng cộng có 44 bệnh nhân được điều trị bằng Casgevy. Trong số 31 bệnh nhân có đủ thời gian theo dõi để đánh giá, có 29 bệnh nhân (93,5%) đạt được kết quả này. Tất cả các bệnh nhân được điều trị đều đạt được sự cấy ghép thành công và không có bệnh nhân nào gặp phải tình trạng ghép thất bại hoặc bị đào thải.
Các tác dụng phụ thường gặp nhất là lượng tiểu cầu và bạch cầu thấp, lở miệng, buồn nôn, đau cơ xương, đau bụng, nôn mửa, sốt giảm bạch cầu (sốt và số lượng bạch cầu thấp), nhức đầu và ngứa.
Dữ liệu hỗ trợ Lyfgenia
Sự an toàn và hiệu quả của Lyfgenia dựa trên phân tích dữ liệu từ một nghiên cứu đa trung tâm kéo dài 24 tháng ở những bệnh nhân mắc bệnh hồng cầu hình liềm và có tiền sử VOE trong độ tuổi từ 12 đến 50 tuổi. Hiệu quả được đánh giá dựa trên độ phân giải hoàn toàn VOE (VOE-CR) trong khoảng từ 6 đến 18 tháng sau khi truyền Lyfgenia. Hai mươi tám (88%) trong số 32 bệnh nhân đạt được VOE-CR trong khoảng thời gian này.
Các tác dụng phụ phổ biến nhất bao gồm viêm miệng (loét miệng ở môi, miệng và cổ họng), lượng tiểu cầu, bạch cầu và hồng cầu thấp, và sốt giảm bạch cầu (sốt và số lượng bạch cầu thấp), phù hợp với hóa trị. và bệnh lý tiềm ẩn.
Bệnh ác tính về huyết học (ung thư máu) đã xảy ra ở những bệnh nhân được điều trị bằng Lyfgenia. FDA có mức cảnh báo cao nhất đối với thông tin liên quan đến rủi ro này. Bệnh nhân nhận được sản phẩm này nên được theo dõi suốt đời đối với các khối u ác tính này.
Cả hai đơn đăng ký của Casgevy và Lyfgenia đều nhận được các chỉ định Đánh giá ưu tiên , Thuốc mồ côi , Theo dõi nhanh và Y học tái tạo .
FDA đã cấp phép Casgevy cho Vertex Pharmaceuticals Inc. và phê duyệt Lyfgenia cho Bluebird Bio Inc.